生物の体の中で物質の化学反応が行われることを「代謝」と言いますが、脂肪の代謝には、ミトコンドリアが関わっています。
健康の鍵を握る脂肪とうまく付き合っていくために、ミトコンドリアと脂肪の関係をご紹介します。
なぜ内臓脂肪の蓄積は体に悪いのか1)
脂肪という言葉を聞いて、楽しい気分になる人は少ないかもしれません。
健康診断の結果や、毎日の体脂肪計の計測結果を思い出してしまうからです。
適度な脂肪は体やホルモンを作るために必要ですが、過剰に体内に蓄積されて肥満になってしまうと、健康にさまざまな悪影響が出ることが知られています。

脂肪の中でも特に注意したいのが、内臓脂肪です。
内臓脂肪はその名の通り、内臓の周りにつく脂肪のことです。
これが蓄積されているとポッコリとお腹が突き出た体型になっていきます。
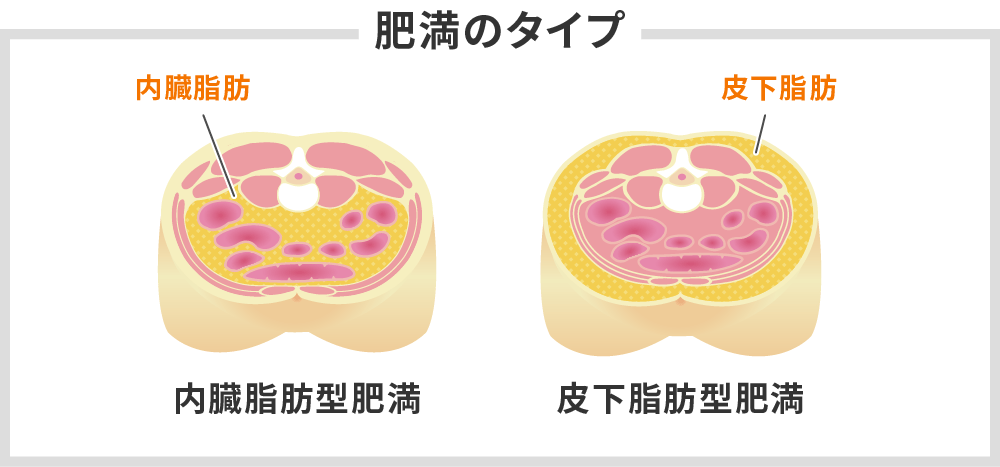
内臓脂肪が多く蓄積している「内臓脂肪型肥満」の人は、皮下脂肪が多い「皮下脂肪型肥満」の人より、糖尿病、高血圧、脂質代謝異常などを発症するリスクが高くなります2)。
内臓脂肪の蓄積が健康に悪い理由は、内臓脂肪をため込む「脂肪細胞」にあります。
脂肪細胞は脂肪を蓄積するだけでなく、体に対して様々なシグナルを分泌する重要な役割を担っています。
ところが、内臓脂肪が増えすぎると、脂肪細胞のシグナルの分泌に異常が起こり、高血圧や高血糖、脂質異常などが起こりやすくなります。
肥満、高血圧、高血糖、脂質異常のうち2つ以上を併せ持った状態をメタボリックシンドロームといい、動脈硬化となるリスクが高まることがわかっています。
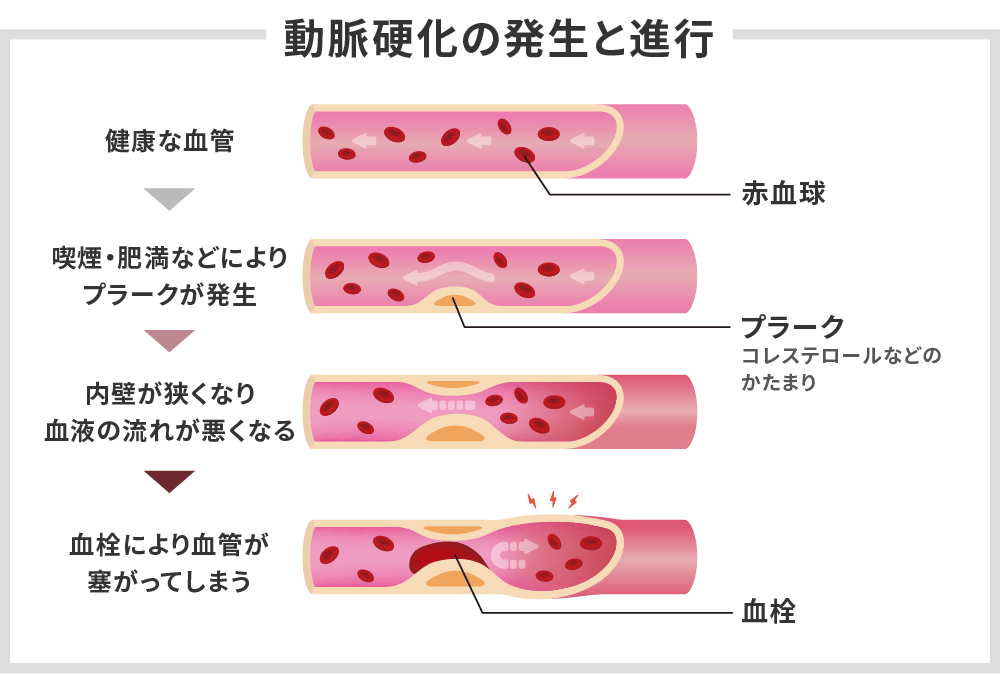
動脈硬化は、動脈の血管が硬くなって弾力性が失われた状態です。
血管内にプラークや血栓が生じて血管が詰まりやすくなり、心筋梗塞や脳梗塞など重篤な病気につながる可能性があるのです。
ミトコンドリアは糖だけでなく脂肪からもエネルギーを作り出す3)
内臓脂肪を減らすためには、脂肪を消費する必要があります。
そこで重要になってくるのがミトコンドリアの働きです。
細胞内でエネルギーを作り出すミトコンドリアは、糖質からエネルギーを作り出すときだけでなく、脂肪からエネルギーを作り出すときにも働いています。
脂肪は科学的には「脂質」とも呼ばれます。
私たちの体に蓄積しエネルギーとして利用される脂質は、トリアシルグリセロールという種類の脂質です。
トリは3のこと。アシルは脂肪酸のこと。つまり、トリアシルグリセロールは、「脂肪酸」3つと「グリセロール」1つが結合した分子です。
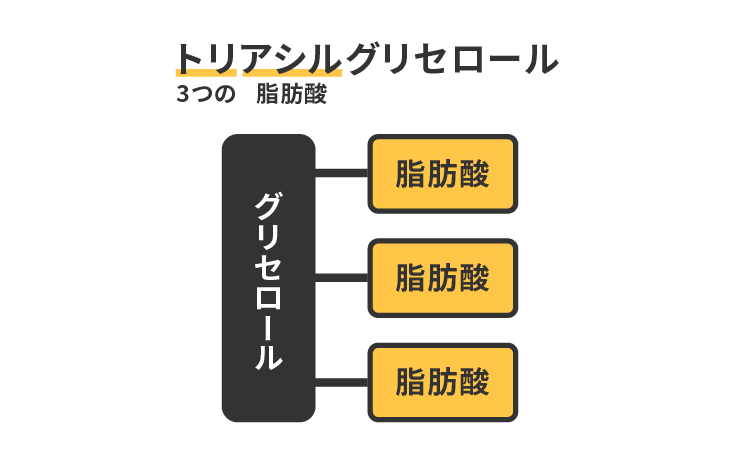
脂質がエネルギーとして使われるための最初のステップは、グリセロールと脂肪酸が分解されて離れ離れになることです。
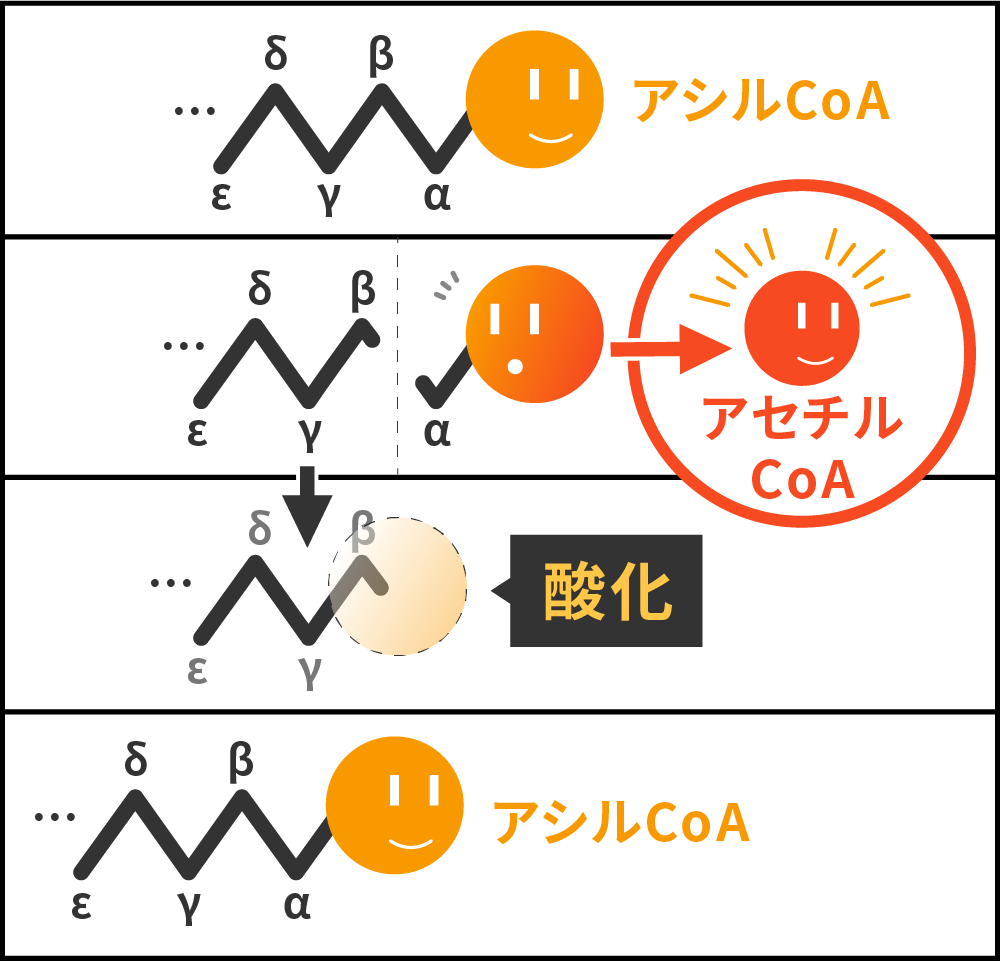
アシルCoAは炭素がたくさん連なった脂肪酸ですが、これを小さく切断すると炭素が2個の「アセチルCoA」が作られます。
ずらりと結合したアシルCoAの炭素の位置は順番にα、β、γと数えますが、2番目の炭素(β)が酸化されて切断されるため、この反応をβ酸化といいます。
アセチルCoAになったら、あとは糖質からエネルギーを作るプロセスと同じです。アセチルCoAは、ミトコンドリアの膜を通過してミトコンドリアのマトリックスに入ります。
そして、ミトコンドリアで行われるTCA回路と呼ばれる一連の化学反応で、細胞のエネルギー源であるATPが作り出されます。
また、切り離されたグリセロールの方もいくつかの化学反応を経て糖質に変換され、脂肪酸と同じようにTCA回路に組み込まれます。
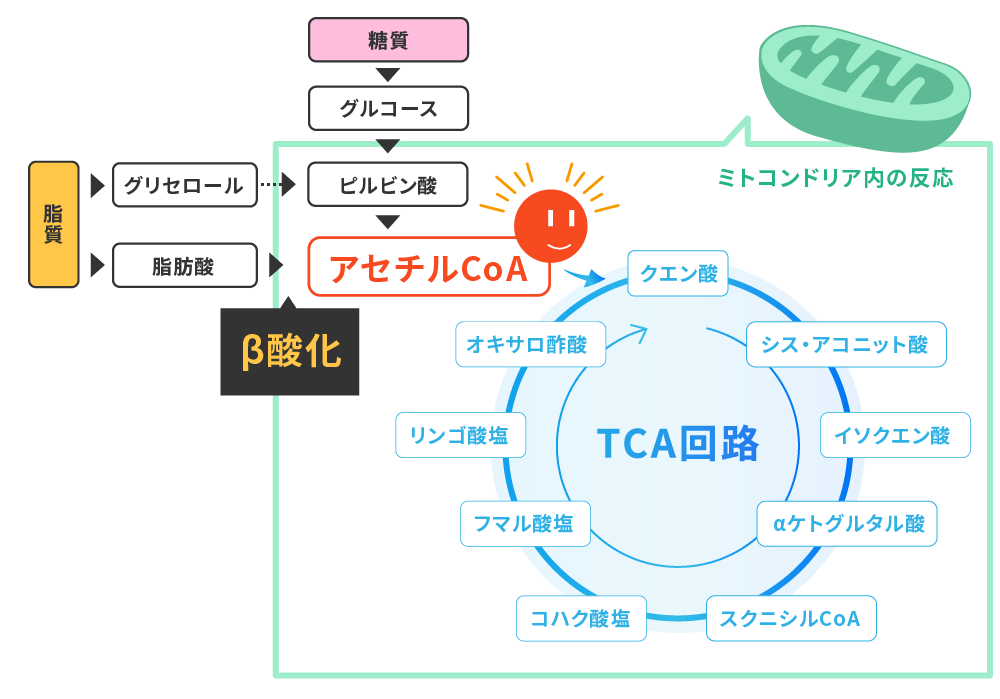
このように脂肪は、グリセロールからも、3つの脂肪酸からもATPを作り出すことができます。
また、1分子の脂肪酸からは、いくつものアセチルCoAを作り出すことができるため、TCA回路を何度も回すことができます。
そのため、脂質から効率よくエネルギーを作り出せます。
蓄積した脂肪を少しでも減らしたい現代人にとっては、あまり直視したくない事実かもしれません。
脂質1gあたりのエネルギー量は9kcalですが、糖質は1gあたり4kcalで、2倍以上も異なります。
しかし、飢餓の危機を何度も乗り越えなければ生き残ることができなかった私たちの祖先にとって、余ったエネルギーを脂肪として蓄えておく仕組みは、命をつなぐための画期的な方法だったに違いありません。
エネルギーを使いきれないと脂肪が合成される3)
運動もせず、エネルギーを使わずに、食事やおやつをたくさん食べていたら、お腹に脂肪はたまっていきます。
この私たちにおなじみの現象を、ミトコンドリアの視点で見てみると、アセチルCoAが余っている状況に相当します。
エネルギーがきちんと消費されれば、TCA回路を回してATPを作る必要がありますが、エネルギーの使いどころがなければ、アセチルCoAは消費されません。
それなのに、食べるのをやめなければ、糖質や脂質からどんどんアセチルCoAが作られてしまいます。
余ったアセチルCoAは、1つ先のクエン酸に変換され、ミトコンドリアの外に出ます。
ミトコンドリアの外に出てもまだそこは細胞の中です。
細胞の中でクエン酸はアセチルCoAに戻り、いくつかの化学反応を経て、中性脂肪が合成されます。
毎日エネルギーが余れば、脂肪は着々と溜まっていきます。
すでにある脂肪を減らしたければ、まずは毎日エネルギーを使い切る必要があります。
運動などで消費するエネルギーを増やし、ミトコンドリアにせっせと働いてもらうしかありません。

もし、ミトコンドリアが働かなくなったら、体はいったいどうなってしまうのでしょうか。
ミトコンドリアの機能が低下すると、代謝が変化し、次のような疾患を引き起こす可能性があることが知られています4)。
- 2型糖尿病
- メタボリックシンドローム
- 肥満
- 脂質異常症
このような疾患が起こる原因のほとんどは、遺伝的にミトコンドリアに障害がある場合です。
しかし、加齢によってミトコンドリアの機能が衰えた場合にも、メタボリックシンドロームの原因になることが研究から示唆されています4) 。
脂肪を燃やす褐色脂肪細胞とミトコンドリア
脂肪は「白色脂肪細胞」と呼ばれる細胞の中に蓄積されます。脂肪細胞の中には「褐色脂肪細胞」と呼ばれる変わり種もいます。褐色脂肪細胞は白色とは逆に、脂肪を燃焼して熱を産生する細胞です。
ミトコンドリアが多く含まれて褐色に見えることから、この名前が付きました。
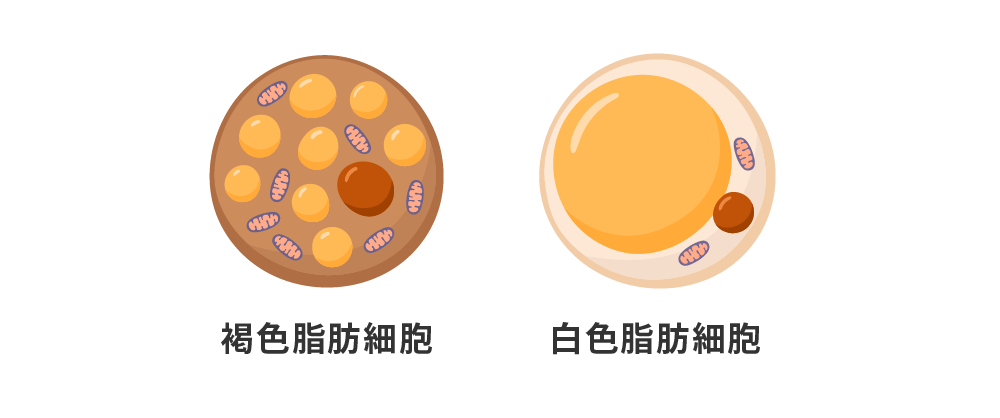
近年、褐色脂肪細胞の働きに注目して肥満の治療を目指す研究が行われています。
遺伝子操作によってミトコンドリアを活性化させたマウスでは、褐色脂肪細胞の働きが活性化され、肥満が抑制される効果が見られたという研究報告もあります5)。
また褐色脂肪細胞には2つの異なる細胞集団があり、筋肉細胞と共通の発生学的起源をもつ古典的な褐色脂肪細胞と、交感神経の刺激で白色細胞から変化して発生する「ベージュ脂肪細胞」があります。
ベージュ脂肪細胞は寒冷刺激が長期間にわたるときに大量に出現し、熱産生を行います6)。
褐色脂肪細胞と同様に、ミトコンドリアを豊富に含む細胞です。
ベージュ脂肪細胞の熱産生は、寒冷刺激やノルアドレナリンの刺激によって行われることが知られています。
2013年にスウェーデンで行われたヒトを対象にした試験では、28人の健康な男女をコントロールと寒冷刺激グループに割り当て、褐色脂肪細胞などの変化を比較しています。
寒冷刺激グループは6週間の間、毎日少なくとも1時間寒さに身をさらしました。具体的には、冷水シャワーを浴びたり、水風呂に入ったり、最高気温が1℃、最低気温が-5℃という2月のスウェーデンのリンシェーピングで薄着のままバルコニーに出たり、窓を開けたりしました。
その結果、寒さを感じないように過ごしたコントロールグループと比べて、代謝率が増加し、ベージュ脂肪細胞の体積が増加していたことが示されました7)。

寒冷刺激がベージュ脂肪細胞を燃焼させるという研究結果は動物やヒトの実験で多く示されており、肥満の治療のターゲットとしてベージュ脂肪細胞が注目されています8)。
ベージュ脂肪細胞にはミトコンドリアが豊富に含まれていることや、白色脂肪細胞のベージュ化はミトコンドリア量やミトコンドリア関連遺伝子発現量と密接に関係しているという報告もある9)ことから、ミトコンドリアと肥満の関係も気になるところです。
三菱ガス化学では、ミトコンドリアを活性化するBioPQQ®が、マウスの脂肪の蓄積を抑制することを示しました(【研究紹介】BioPQQ®はマウスの脂肪の蓄積を抑制する)。
ヒトについての効果は、現在研究を進めています。
新しい知見や研究成果が出ましたらコラムで紹介していきますので、ぜひ今後も脂肪とミトコンドリアの関係について、注目してください。
参考
1) 近藤和雄『人のアブラはなぜ嫌われるのか -脂質「コレステロール・中性脂肪など」の正しい科学』2015年(技術評論社)
2) 厚生労働省 e-ヘルスネット 肥満と健康
https://www.e-healthnet.mhlw.go.jp/information/food/e-02-001.html
3) 田中文彦『忙しい人のための代謝学』2020年(羊土社)
4) Mohanty A, Tiwari-Pandey R, Pandey NR. Mitochondria: the indispensable players in innate immunity and guardians of the inflammatory response. J Cell Commun Signal. 2019 (3):303-318. doi: 10.1007/s12079-019-00507-9.
5) Masakazu Fujii, Daiki Setoyama, Kazuhito Gotoh, Yushi Dozono, Mikako Yagi, Masataka Ikeda, Tomomi Ide, Takeshi Uchiumi, Dongchon Kang, TFAM expression in brown adipocytes confers obesity resistance by secreting extracellular vesicles that promote self-activation(2022) iScience Vol 25, Issue 9 DOI:https://doi.org/10.1016/j.isci.2022.104889
6) 斉藤昌之(2020)「褐色脂肪組織による熱産生と体温・体脂肪調節」Jpn J Psychosom Med 60 210-216
https://www.jstage.jst.go.jp/article/jjpm/60/3/60_210/_pdf
7) Romu T, Vavruch C, Dahlqvist-Leinhard O, Tallberg J, Dahlström N, Persson A, Heglind M, Lidell ME, Enerbäck S, Borga M, Nystrom FH. A randomized trial of cold-exposure on energy expenditure and supraclavicular brown adipose tissue volume in humans. Metabolism. 2016;65(6):926-34. doi: 10.1016/j.metabol.2016.03.012.
8) Huo C, Song Z, Yin J, Zhu Y, Miao X, Qian H, Wang J, Ye L, Zhou L. Effect of Acute Cold Exposure on Energy Metabolism and Activity of Brown Adipose Tissue in Humans: A Systematic Review and Meta-Analysis. (2022) Front Physiol. 13:917084. doi: 10.3389/fphys.2022.917084.
9) 米代 武司,梶村 真吾(2017) 褐色脂肪細胞およびベージュ脂肪細胞の制御機構と臨床的意義
Journal of Japanese Biochemical Society 89(6): 917-920
doi:10.14952/SEIKAGAKU.2017.890917




