医療の発展や衛生状態の改善により、平均寿命は年々伸び続けています。特に長寿国である日本の平均寿命は、2004年は男性が78.64歳、女性が85.59歳1)でしたが、2024年には男性が81.09歳、女性が87.13歳と直近の20年間でも大きく伸びています。
一方、最高寿命の世界記録は1997年の122歳2)で、120歳を越えて生きることは現代でも難しいことがわかります。そのため、長らくの間、寿命は変えられないものであり、老化は避けられない現象だと考えられてきました。
しかし近年の研究によって、老化には単なる時間の経過だけでなく、特定の遺伝子や細胞の仕組みが深く関わっていることが明らかになってきました。老化の原因となるメカニズムを理解すれば、健康寿命を延ばしたり、老化に伴う病気を予防したりできるかもしれないという期待が高まっています。
その中でも注目を集めているのが「サーチュイン遺伝子」です。サーチュインは、細胞内でエネルギーの利用やDNAの修復、ストレス応答の調節に関わる酵素をコードしており、老化や寿命と密接に関わることが示されています。動物実験では、サーチュインの働きを高めることで寿命や健康状態を改善する例も報告されています。
この記事では、老化のメカニズムの基本を紹介しながら、サーチュイン遺伝子がどのように寿命や健康を制御するのかを解説します。
老化とは「死にやすくなる現象」
「老化」という言葉は日常生活の中でさまざまな意味で使われます。美容の分野ではシワや白髪の出現を指し、健康の面ではよく体力や持久力の低下、代謝の低下などが「老化」と表現されます。
生物学的に定義すると、老化は、「年齢とともに死亡のリスクが増していく現象」です。たとえば事故に遭遇する確率は年齢に比例しませんが、心血管疾患や神経変性疾患の発症率は加齢とともに上昇します。また、感染症にかかる確率自体は全年齢で一定ですが、高齢者では免疫機能が低下するため、重症化や死亡のリスクは大きく高まります。
特に、加齢性疾患と呼ばれる病気は典型的です。動脈硬化や心筋梗塞のような心血管疾患、アルツハイマー病やパーキンソン病のような神経変性疾患、糖尿病などの生活習慣病は、ある年齢を超えると発生率が一気に上昇します。
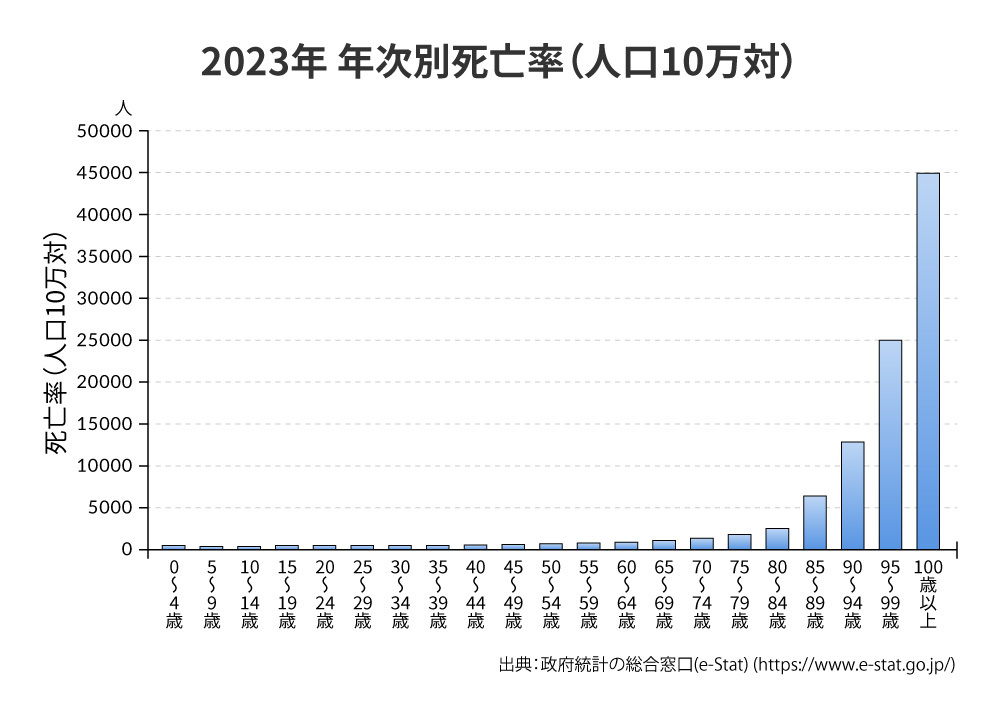
このような病気が重なりや体力の低下など、死因はさまざまですが、人間の死亡率は30~40歳以降から指数関数的に上昇し、70歳を越える頃にはその傾向が一層強まり、死亡率は急激に上昇していきます(下図)3)。つまり老化とは単なる外見上の変化ではなく、生存率そのものが下がっていき「死にやすくなる現象」といえるのです。
抗老化のカギは細胞の修復力にある
家電製品は長年使っていると部品が摩耗して故障してしまいます。では、私たちの体の部品(=細胞やその中の分子)も時間とともに壊れてしまうのでしょうか。
機械と生物の大きな違いは、生物が絶えず変化し続ける存在だという点です。私たちは外から栄養を取りこみ、常に代謝を繰り返しています。そのため、生物の「部品」は作られては使われ、壊れたり修復されたりを繰り返しており、機械の部品よりもはるかに動的で壊れやすい状態にあります。
こうした不安定さに対応するため、生物は壊れたDNAを修復したり、機能不全を起こした細胞を取り除いたりといった修復・防御の仕組みを備えています。ただし、これらが常に完璧に働くわけではありません。長い時間をかけて修復しきれなかったダメージは少しずつ蓄積していきます。また、加齢とともに修復機能そのものも衰えていき、その結果として細胞や組織の不具合が増え、老化へとつながっていくのです。
代表的な修復・防御機能には次のようなものがあります。
- DNA修復機構:
遺伝子の損傷を修復し、突然変異を発生を抑える - タンパク質品質管理:
正しく折りたたまれなかったタンパク質を分解したり、再び折りたたんだりする - アポトーシス:
修復不能な細胞を自発的に死滅させ、がん化や炎症から組織全体を守る - オートファジー:
細胞内の不要なタンパク質や損傷したオルガネラを分解し、資源として再利用する
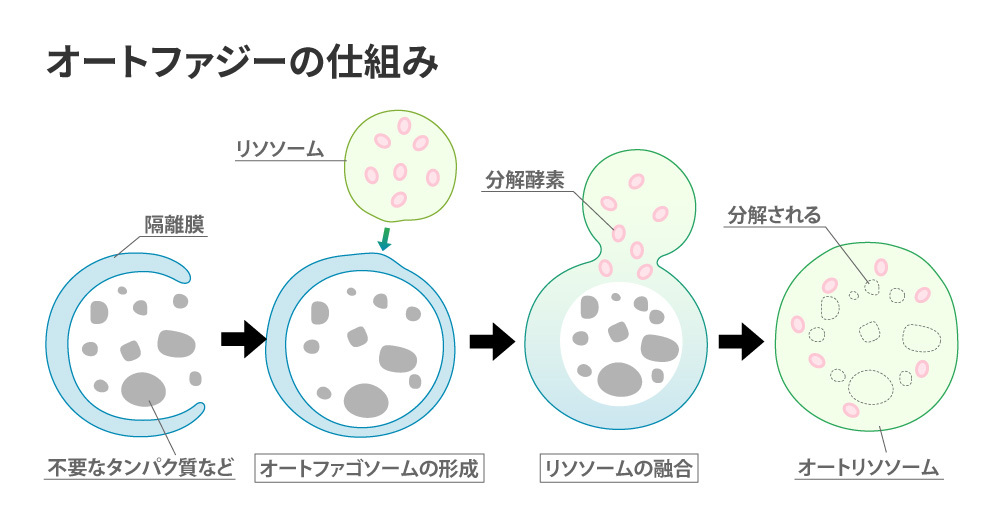
これらの修復・防御機能に関わる遺伝子や分子は、老化を抑制するカギを握る可能性があると考えられ、世界中で盛んに研究されています。その代表例のひとつが、「サーチュイン遺伝子」です。サーチュインは特にDNAの修復や安定性を保つ仕組みと深く関わっていることが知られており、老化研究の重要なターゲットとなっています。

長寿遺伝子サーチュインをサポートする食品
サーチュインはもともと酵母で発見されましたが、その後、線虫やショウジョウバエ、マウス、さらにはヒトに至るまで、進化の過程を越えて保存されていることがわかりました。
酵母や線虫、ショウジョウバエ、マウスといった動物実験では、サーチュインの発現量を増やすと寿命が延びるという結果が報告されています。ただし、ヒトについてはまだ結論が出ていません。ヒトの寿命は非常に長いため、寿命そのものが延びるかどうかを科学的に確認するには数十年単位の研究が必要だからです。
一方で、サーチュインが健康状態の改善や加齢関連疾患の予防に役立つ可能性は数多くの研究から示されています。そのため、サーチュインの働きをサポートする健康補助食品が注目を集め、世の中に広がりつつあります。
サーチュインの働きを支える可能性のある食品として、次のようなものが報告されています。
1)NR(ニコチンアミドリボシド)、
NMN(ニコチンアミドモノヌクレオチド)
これらはNAD+の前駆体です。サーチュインが機能するためには、細胞内に存在する補酵素NAD+(ニコチンアミドアデニンヌクレオチド)が不可欠ですが、NAD+は加齢に伴って減少することが知られています。NAD+そのものを食品として摂取しても、消化の過程で分解されやすく、さらに分子が大きいため細胞内には取り込みにくいことが知られています。NAD+の材料となるNRやNMRを経口摂取するとNAD+が増えることが研究によって確かめられています4)。
2)レスベラトロール
赤ワインに含まれるポリフェノールの一種で、抗酸化作用をもちます。サーチュインの活性化作用があるとして注目されてきましたが、研究結果は必ずしも一貫しておらず、効果については議論が続いています。
3)PQQ(ピロロキノリンキノン)
ミトコンドリア機能をサポートする補酵素の一つです。三菱ガス化学が提供するBioPQQを用いた培養細胞試験では、BioPQQが細胞内のNAD+を増加させる効果を示し、NMNの約5000分の1という少量での作用が認められました。ただし、この結果は細胞実験に基づくものであり、ヒトでの効果については今後の研究が必要です。

ヒトの寿命研究はこれからだが抗老化には期待
ヒトは寿命が長いため研究が容易ではありませんが、老化のメカニズムが少しずつ解明されることで、加齢に伴う病気を予防できる可能性が見えてきています。
本記事で取り上げたDNA修復機構に加え、オートファジーやアポトーシスを支える仕組みを活用した老化防止研究も進展しています。また修復機構だけでなく、ミトコンドリア機能の低下によって生じる細胞ダメージも老化に深く関わることも明らかになってきました。
BioPQQはサーチュインの働きを支えるだけでなく、ミトコンドリアの新生を促す作用があることが報告されています。さらに、ミトコンドリアのオートファジーであるマイトファジーの健全化にも寄与すると報告されています。こうした複数の側面からBioPQQが抗老化に貢献する可能性が期待されます。実際に、まだメカニズムは不明なところもありますが、BioPQQを摂取した線虫で寿命の延長が確かめられていたり5)、老化促進モデルマウスにおいてBioPQQ摂取が老化変化を抑制する6)という研究結果も出ています。
生物として生まれた以上、死という運命そのものを避けることはできません。しかし、なるべく長く健康でいたいという願いは、今後の研究の進展によって現実に近づいていくかもしれません。

参考文献
1) 内閣府 平成18年高齢化社会白書
https://www8.cao.go.jp/kourei/whitepaper/w-2006/zenbun/html/i1131000.html
2)「人間は何歳まで生きられる? 寿命決める遺伝子とは」NIKKEI STILE 2016年2月15日(日本経済新聞)
3) 政府統計の総合窓口(e-stat)
https://www.e-stat.go.jp/
4) デビッド・A・シンクレア、マシュー・D・ラプラント(2020)『LIFE SPAN 老いなき世界』 東洋経済新報社
5) Sasakura H, Moribe H, Nakano M, Ikemoto K, Takeuchi K, Mori I. Lifespan extension by peroxidase and dual oxidase-mediated ROS signaling through pyrroloquinoline quinone in C. elegans. J Cell Sci. 2017 Aug 1;130(15):2631-2643. doi: 10.1242/jcs.202119. Epub 2017 Jul 4. PMID: 28676501.
6) 高橋良哉「ピロロキノリンキノン(PQQ)とイミダゾピロロキノリン(IPQ)の 投与がマウスの老性変化と寿命に与える影響」第25回日本抗加齢医学会総会 口頭演題O16-1、2025年6月13日




