サプリメントの健康被害問題をめぐり、機能性表示食品がニュースなどで話題になっています。この記事では、食品の表示のルールや知っておくべきことについて、分かりやすく解説していきます。
食品は勝手に機能を表示できない
食品を販売する事業者にとって、製品のパッケージや広告の文言は、消費者に自分たちの製品の魅力を伝える重要なツールです。事業者たちは、自分たちの製品が消費者にとって有益であることを、言葉やデザインでさまざまに表現しようとします。
ところがもし、その表現に誇張や噓や誤解させるような内容が混じってしまうと、消費者が不利益を被ります。消費者の正しい判断を可能にするためには、事業者に行き過ぎた表現を禁止し、必要な情報が隠されないように求めることが有効です。
そういったことから国は、消費者の利益を守るために食品表示法などの法律を設け、必ず表示しなければならない事項(義務表示)や、許可なく表示してはいけない内容などを定めています。

必ず記載しなければならない義務表示には、たとえば、アレルゲン、消費期限、保存方法、名称、原材料、原産地、添加物、内容量、栄養成分などがあります。
事業者が判断して記載する任意表示については、景品表示法や薬機法という別の法律によって、書いてはいけないことが定められています。
特に、食品の成分によって健康増進の効果を期待する健康食品は、科学的根拠がないのに「病気が治る」といった内容が記載されていると、消費者に大きな不利益をもたらします。そのため、食品の表示には特別な認可を得ない限り、効果や効能などの「機能性 」を記載することはできません。
機能を表示できる特別な認可を得た食品を「保健機能食品」と呼びます。その中には「特定保健用食品(トクホ)」、「栄養機能食品」があり、健康被害の問題で話題になっている「機能性表示食品」も含まれます。
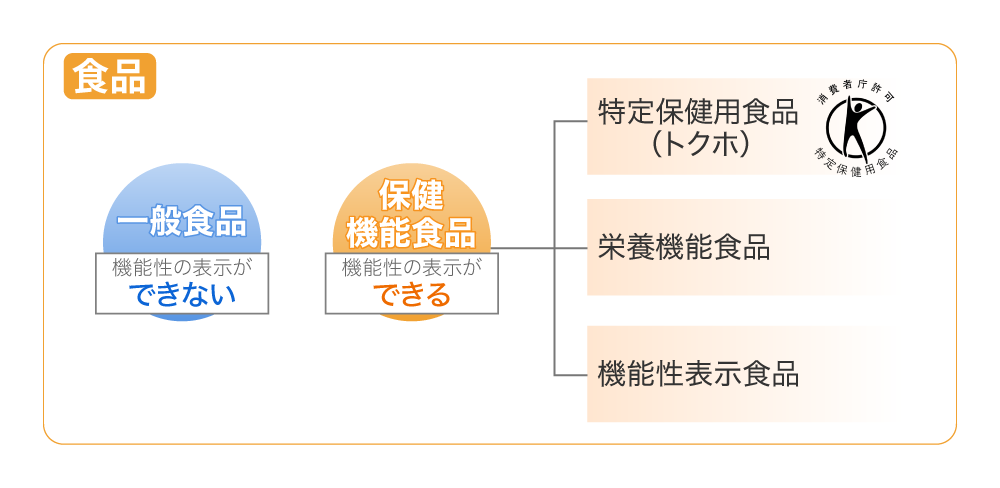
一般食品の中にも、健康増進の効果を期待できる製品はありますが、認可がない限り機能性を表示することはできません。たとえば、アンチエイジング効果が期待される食品であっても、一般食品であれば「老化を予防する」などと表示することはできず、「若々しくありたい方に」といった記載にとどまることになります。
栄養補助食品、健康補助食品といった表示で販売されている食品も一般食品なので、機能性を表示することはできません。
では、機能性を表示できる保健機能食品は、どのようなプロセスを経て販売されているのでしょうか。
トクホと機能性表示食品の違い 1)
人が両手を挙げて伸びをしているマークが目印の特定保健用食品、いわゆるトクホは、1991年にスタートした制度です。トクホは、国が、人での安全性と効果を個別に審査します。
また、栄養機能食品は、亜鉛、カリウム、カルシウム、ビタミンなど、科学的根拠が確認された栄養成分について、国が定めた一定の基準量を含んでいれば栄養成分の機能を表示することができる制度で、2001年に制定されました。
保健機能食品のなかで、最も新しい制度が、機能性表示食品で、2015年からスタートしました2)。
機能性表示食品は、トクホと同様に、臨床試験やシステマティックレビューという、科学的検証を必要とする一方、個別審査を有するトクホほど審査に費用と時間がかかりません。そのため、商品の開発から販売のスピード面では機能性表示食品に優位性があり、大企業でなく中小企業にも、道が開かれた制度です。
機能性表示食品の販売を行う際、事業者は自らの責任で、効果の科学的根拠や安全性などの要件を満たしていることを示す資料を用意し、国に提出します。受理された届出は消費者庁のウェブサイトで公開されます。
この制度によって、トクホや栄養機能食品の表示にはなかった機能が表示できるようになりました。たとえば、認知機能、睡眠、目、肌、ストレス、疲労感などです。

機能性表示食品は信頼できないのか
健康被害の問題を受けて、機能性表示食品はトクホと違って国が個別に認可していないことを初めて知った人も多いでしょう。しかし、だからといって、機能性表示食品すべてが信頼できない制度だと結論づけるのは、まだ早いかもしれません。
機能性表示食品の届け出に必要な資料は、届け出が受理されたあとに消費者庁のウェブサイトに開示されます。消費者は製品に付記されている「届出番号」をもとに、科学的根拠となる資料を見ることができます。専門外の人には資料のすべてを理解することは難しいかもしれませんが、分かる人が見れば資料が信頼できるものかどうかは分かります。いい加減な資料であれば、事業者としての信頼も失うことになります。
また、機能性表示食品の表示の仕方にも細かな決まりがあります。科学的な根拠で示された範囲から逸脱した表示とならない表現にとどめたり、医薬品ではないことや国から個別の審査を受けたものではないことなども記載したりしなくてはなりません。
機能性表示食品は、トクホよりも審査のハードルが低い制度と考えられがちではありますが、決して科学的根拠の質が低いわけではありません。むしろ、一定の基準を満たす資料が必要なことや、届け出された資料が公開されることを考えれば、消費者の判断に役に立つ制度といえます。
正しく利用するためには、消費者が制度を理解することが必要です。さらに、これはトクホも同じですが、表示さえあれば何もかもが保障されるというわけではありません。生産や流通の過程で問題が起きることもあります。問題が起きたときにどのように対応するか、企業の姿勢が問われています。
機能性表示食品の健康被害の問題を受け、政府は制度の見直しを行いました3)。具体的には、医師などから健康被害と疑われる情報が寄せられた際、一定の条件を満たす場合は因果関係が不明でもすぐに国に報告することや、サプリメントを加工する工場では医薬品で用いられるような厳正な基準(GMP)に基づいた製造管理をすることなどです。また、専門家会議を設置して、新たな機能性関与成分を届け出があったときには専門家の意見を聞く仕組みを導入することも検討されています。
以前よりも安心して利用できるようになった機能性表示食品。トクホや一般食品との違いを理解した上で、上手く付き合っていきたいものです。
機能性食品の届け出の例:BioPQQ®を使った製品の場合
最後に、機能性食品の届け出が受理されるためには、どのような資料が必要なのかを、BioPQQ®を原料とした機能性食品を例に、説明します。
BioPQQ®を原料に使用した食品が届け出によって記載できるようになった表示は、次のような文言です。
「本品はピロロキノリンキノン二ナトリウム塩を含んでいます。ピロロキノリンキノン二ナトリウム塩は、健康な中高齢者に対して、認識能力の一部である注意力及びワーキングメモリー(得られた視覚情報を短時間で認識し、同時に正しく処理し行動に移す能力)の維持に役立つことが報告されています。」
製品のパッケージには以下のように機能性を表示することができます。

トクホでは機能性の評価方法として、製品を用いた臨床試験が必要ですが、機能性食品の場合は、①最終製品を用いた臨床試験(ヒト試験)、②最終製品又は機能性関与成分に関する研究レビューのいずれかを提示することになります。②の場合必ずしも自社で行った研究ではなくてもよいですが、届出者だけでなく世界中の研究機関から報告された試験データを総合的に評価する必要があり、質の高い臨床試験の症例数が多いことが望まれます。
コラムでも紹介しているように、BioPQQ®に関してはさまざまな研究が行われ、科学的知見が蓄積しています。また、三菱ガス化学でもBioPQQ®を摂取する臨床試験を行い、その効果を確かめています。
自社で研究開発を行っている三菱ガス化学は、BioPQQ®を用いた製品を機能性食品として届け出るためのサポート体制が充実しています。最終製品を作る企業と協力して、消費者の方々の信頼に応えられる製品を、これからも作り続けていきます。

※機能性表示食品の届け出の内容の詳細は、製品に記載されている届け出番号を消費者庁の検索画面に入力することで、閲覧することができます。
参考
1) 厚生労働省 eヘルスネット「特保(特定保健用食品)とは?」 https://www.e-healthnet.mhlw.go.jp/information/food/e-01-001.html
2) 消費者庁 「機能性表示食品って何?」 https://www.caa.go.jp/notice/assets/150810_1.pdf
3) 厚生労働省 参考資料「機能性表示食品を巡る検討会 報告書」令和6年5月27日 https://www.mhlw.go.jp/content/12401000/001257980.pdf




